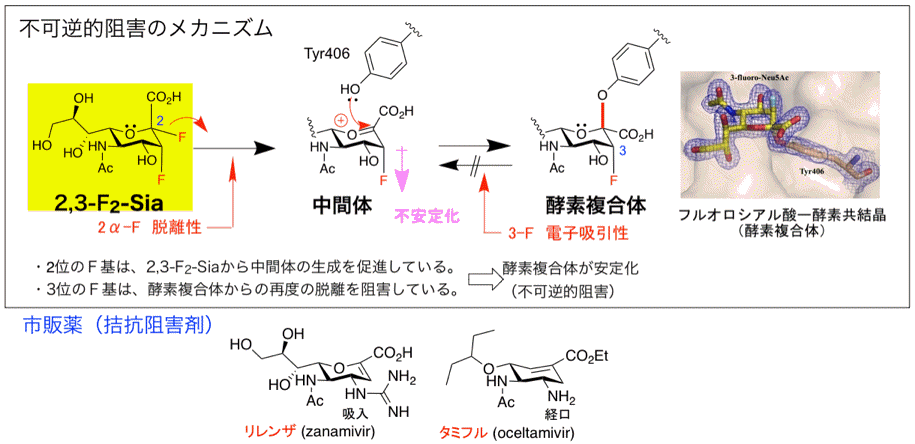
・2,3-ジフルオロシアル酸(2,3-F2-Sia)を用いて、インフルエンザウィルスのシアリダーゼが、保持型のグリコシダーゼであることを明らかにしました。
・2,3-F2-Siaが、シアリダーゼ活性中心のTry406残基と共有結合を形成し、不可逆的阻害剤としてはたくことを明らかにしました。
・2,3-F2-Siaは、B型インフルエンザ酵素にはリレンザと同等の阻害効果を、またタミフル耐性株酵素にも強力に阻害効果を示しました。
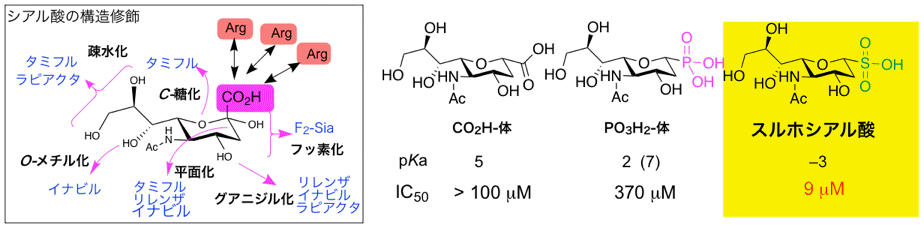
これまで下図の様にシアル酸を鋳型に数多くの官能基置換が試みられてきました。我々はこれまでの上市薬では例のない1位カルボキシ基の置換を検討しました。ホスホノ基の導入が有効との知見から、さらに酸性度の強いスルホ基ならば、酵素活性中心の3個のアルギニン残基と相互作用も強くなると予想し、スルホシアル酸を設計、合成を達成しました。スルホシアル酸は、カルボキシ体やホスホノ体の数十倍強い活性を示し、スルホ基が次世代阻害剤の置換基として有望と分かりました。
257. "抗インフルエンザ薬開発を指向したシアル酸誘導体(シアリダーゼ阻害剤)の開発"
[REVIEW]
256. "Influenza A Virus Neuraminidase Inhibitors - Recent Progresses -" [REVIEW]
255. "Synthesis and Neuraminidase Inhibitory Activity of Sialic Acid Analogs with Fluoro, Phosphono, or Sulfo Functionality" [REVIEW]
237. "アノマー位置換による不可逆的シアリダーゼ阻害剤の開発" [REVIEW]
237. "Towards Improvement of Covalent NA Inhibitors with Anomeric Substitution" [REVIEW]
219. "Synthesis of Sulfo-Sialic Acid Analogues: Potent Neuraminidase Inhibitors in Regards to Anomeric Functionality"
187. "Functional and Structural Analysis of Influenza Neuraminidase N3 Offers Further Insight into the Mechanisms of Oseltamivir Resistance"
184. "Influenza Neuraminidase Operates via a Nucleophilic Mechanism and can Be Tageted by Covalent Inhibitors"
C. J. Vavricka, 清田洋正, 科学と工業, 97, 2-7 (2023)
N. Sriwilaijaroen, C. J. Vavricka, H. Kiyota, Y. Suzuki, Methods Mol. Biol., 2556, 321-353 (2020), 10.1007/978-1-0716-2635-1_21
C. J. Vavricka, N. Sriwilaijaroen, Y. Suzuki, H. Kiyota, Methods Mol. Biol., 2556, 303-320 (2020), 10.1007/978-1-0716-2635-1_20
クリストファー・ヴァヴリッカ, 松本達磨, 清田洋正, Trends Glycosci. Glycotech., 32(184), J1-J5 (2020), 10.4052/tigg.1801.1J
C. J. Vavricka, T. Matsumoto, H. Kiyota, Trends Glycosci. Glycotech., 32(184), E1-E5 (2020), 10.4052/tigg.1801.1E
C. J. Vavricka, C. Muto, T. Hasunuma, Y. Kimura, M. Araki, Y. Wu, G. F. Gao, H. Ohrui, M. Izumi, H. Kiyota , Sci. Rep., 7, 8239 (2017), 10.1038/s41598-017-07836-y
Pat-11. "シアル酸誘導体、その製造方法及びそれを利用したシアリダーゼ阻害剤、抗菌剤、抗ウイルス剤"
清田洋正,クリストファー・ヴァヴリカ, 特許6871587(2021/04/20).
Q. Li, J.-X. Qi, Y. Wu, H. Kiyota, K. Tanaka, Y. Suhara, H. Ohrui, Y. Suzuki, C. J. Vavricka, G. F. Gao, J. Virol., 87(18), 10016-10024 (2013), 10.1128/JVI.01129-13
C. J. Vavricka, Y. Liu, H. Kiyota, N. Sriwilajiaroen, J.-X. Qi, K. Tanaka, Y. Wu, Q. Li, Y. Li, J.-H. Yan, Y. Suzuki, G. F. Gao Nat. Commun., 4, 1491 (2013), 10.1038/ncomms2487.